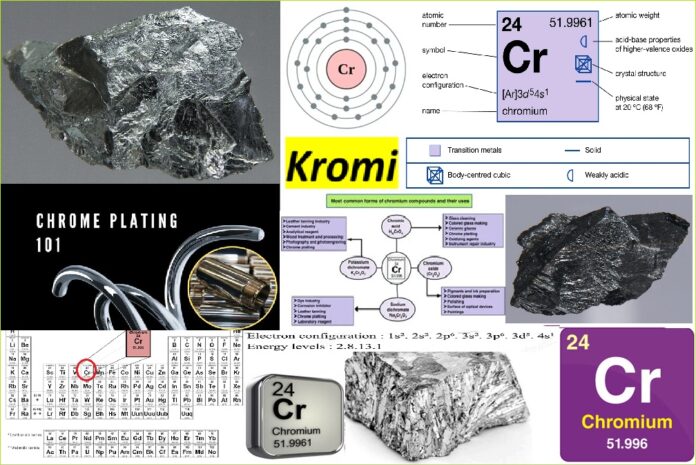
Kromi është një element kimik; ka simbolin Cr dhe numrin atomik 24. Përfaqësohet në periudhën 4, grupi 6, blloku d, në Tabelën Periodike. Është elementi i parë në grupin 6. Është një metal tranzicioni gri i çeliktë, i shkëlqyeshëm, i fortë dhe i brishtë.
[: Kromi vlerësohet për rezistencën dhe fortësinë e tij të lartë ndaj korrozionit. Një zhvillim i madh në prodhimin e çelikut ishte zbulimi se çeliku mund të bëhej shumë rezistent ndaj korrozionit dhe çngjyrosjes duke shtuar krom metalik për të formuar çelik inox. Çeliku inox dhe kromi (galvanizimi me krom) së bashku përbëjnë 85% të përdorimit komercial. Kromi vlerësohet gjithashtu shumë si një metal që mund të lëmohet shumë duke i rezistuar njollosjes. Kromi i lëmuar reflekton pothuajse 70% të spektrit të dukshëm dhe pothuajse 90% të dritës infra të kuqe. Emri i elementit rrjedh nga fjala greke χρῶμα, chrōma, që do të thotë ngjyrë, sepse shumë komponime të kromit janë me ngjyra intensive.]1
Prodhimi i Kromit
Prodhimi industrial i kromit vazhdon nga minerali i kromitit (kryesisht FeCr2O4) për të prodhuar ferrokrom, një aliazh hekuri-kromi, me anë të reaksioneve aluminotermike ose silikotermike. Ferrokromi përdoret më pas për të prodhuar lidhje të tilla si çeliku inox. Metali i pastër i kromit prodhohet nga një proces tjetër: pjekja dhe kullimi i kromitit për ta ndarë atë nga hekuri, i ndjekur nga reduktimi me karbon dhe më pas alumin.
Vetitë
| Kromi: 24Cr, Grupi 6, Periudha 4, Blloku D, Metal |
| Pamja: metalik argjendi |
| Numri atomik (Z): 24 |
Pesha standarde atomike Ar°(Cr): 51.9961±0.0006, • 51.996±0.001 (shkurtuar) |
| Konfigurimi i elektroneve: [Ar] 3d5 4s1 |
| Elektronet për guaskë 2, 8, 13, 1 |
| Vetitë fizike |
| Faza në STP: e fortë |
| Pika e shkrirjes: 2180 K (1907 °C, 3465 °F) |
| Pika e vlimit: 2944 K (2671 °C, 4840 °F) |
| Dendësia: (në 20° C): 7.192 g/cm3, kur është i lëngshëm (në MP): 6.3 g/cm3 |
| Nxehtësia e shkrirjes: 21.0 kJ/mol |
| Nxehtësia e avullimit: 347 kJ/mol |
| Kapaciteti i nxehtësisë molare: 23.35 J/(mol· K) |
| Kapaciteti specifik i nxehtësisë: 449.073 J/(kg· K) |
| Vetitë atomike |
| Shtetet e oksidimit. E zakonshme: +3, +6, (−4, −2, −1, 0, +1, +2, +4, +5) |
| Elektronegativiteti, Shkalla Pauling: 1.66 |
| Energjitë e jonizimit: • 1: 652.9 kJ/mol, • 2: 1590.6 kJ/mol, • 3: 2987 kJ/mol, • (më shumë) |
| Numri CAS: 7440-47-3 |
| Histori |
| Emërtimi: nga greqishtja χρῶμα, “ngjyrë“, sepse shumë komponime të kromit janë me ngjyra intensive. |
| Zbulimi dhe izolimi i parë: Louis Nicolas Vauquelin (1794, 1797) |
| Izotopet kryesore: 50Cr, bollëk 4.34%, gjysma e jetës (t1/2): e qëndrueshme. 51Cr, sintetizator, gjysma e jetës (t1/2): 27.7015 d. 52Cr, bollëk 83.8%, gjysma e jetës (t1/2): e qëndrueshme. 53Cr, bollëk 9.50%, gjysma e jetës (t1/2): e qëndrueshme. 54Cr, bollëk 2.37%, gjysma e jetës (t1/2): e qëndrueshme. |
| – |
Kromi trevalent (Cr(III)) ndodh natyrshëm në shumë ushqime dhe shitet si një shtesë dietike, megjithëse nuk ka prova të mjaftueshme që kromi dietik ofron përfitime ushqyese për njerëzit. Në vitin 2014, Autoriteti Evropian i Sigurisë Ushqimore arriti në përfundimin se hulumtimi mbi kromin dietik nuk justifikonte njohjen e tij si një lëndë ushqyese thelbësore.
Ndërsa metali i kromit dhe jonet Cr (III) konsiderohen jo toksike, kromati dhe derivatet e tij, shpesh të quajtura “kromi gjashtëvalent”, janë toksike dhe kancerogjene. Sipas Agjencisë Evropiane të Kimikateve (ECHA), trioksidi i kromit që përdoret në proceset industriale të galvanizimit është një “substancë me shqetësim shumë të lartë” (SVHC).
Ndodhia, përdorimet e kromit
[Britannica:2
Kromi (Cr), element kimik i Grupit 6 (VIb) i tabelës periodike, një metal i fortë çeliku-gri që merr një lustrim të lartë dhe përdoret në lidhje për të rritur forcën dhe rezistencën ndaj korrozionit. Kromi u zbulua (1797) nga kimisti francez Nicolas-Louis Vauquelin dhe u izolua si metal një vit më vonë; ajo u emërua për komponimet e saj shumëngjyrëshe. Ngjyra jeshile e smeraldit, gjarpërinjve dhe mikës së kromit dhe ngjyra e kuqe e rubinit janë për shkak të sasive të vogla të kromit. Emri i elementit krom (nga greqishtja chrōmos, “ngjyrë”) nënkupton ngjyrat e theksuara dhe të larmishme të komponimeve të kromit.
Kromi është një element relativisht i bollshëm në koren e Tokës; Metali i lirë nuk gjendet kurrë në natyrë. Shumica e mineraleve përbëhen nga kromiti mineral, formula ideale e të cilit është FeCr2O4. Është i shpërndarë gjerësisht në depozita natyrore, të cilat zakonisht janë të kontaminuara me oksigjen, magnez, alumin dhe silicë; përmbajtja e tyre e kromit varion nga 42 në 56 përqind. Një nga përdorimet kryesore të kromit është në lidhjet e hekurta, për të cilat metali i pastër nuk kërkohet. Prandaj, kromiti shpesh reduktohet me karbon në një furrë, duke prodhuar aliazhin ferrokrom, i cili përmban hekur dhe krom në një raport atomi afërsisht 1 me 2.
Për të marrë krom të pastër, kromiti fillimisht trajtohet me alkali dhe oksigjen të shkrirë, duke shndërruar të gjithë kromin në kromat alkali, dhe ky i fundit tretet në ujë dhe përfundimisht precipitohet si dikromat natriumi, Na2Cr2O7. Dikromati më pas reduktohet me karbon në sesquioxide kromi, Cr2O3, dhe ai oksid nga ana tjetër reduktohet me alumin për të dhënë metalin e kromit.
Kromi i shtohet hekurit dhe nikelit në formën e ferrokromit për të prodhuar lidhje të karakterizuara posaçërisht nga rezistenca e tyre e lartë ndaj korrozionit dhe oksidimit. Përdoret në sasi të vogla, kromi ngurtëson çelikun. Çeliqet inox janë lidhje të kromit dhe hekurit në të cilat përmbajtja e kromit varion nga 10 në 26 përqind. Lidhjet e kromit përdoren për të fabrikuar produkte të tilla si tubat e vajit, veshjet e automobilave dhe takëmet. Kromiti përdoret si zjarrdurues dhe si lëndë e parë për prodhimin e kimikateve të kromit.
Metali është i bardhë, i fortë, i shkëlqyeshëm dhe i brishtë dhe është jashtëzakonisht rezistent ndaj reagentëve të zakonshëm gërryes; Kjo rezistencë shpjegon përdorimin e saj të gjerë si një shtresë mbrojtëse e galvanizuar. Në temperatura të larta kromi bashkohet drejtpërdrejt me halogjenët ose me squfurin, silikonin, borin, azotin, karbonin ose oksigjenin. (Për trajtim shtesë të metalit të kromit dhe prodhimin e tij, shih përpunimin e kromit.)
Kromi natyral përbëhet nga një përzierje e katër izotopeve të qëndrueshme: krom-52 (83.76 përqind), krom-53 (9.55 përqind), krom-50 (4.31 përqind) dhe krom-54 (2.38 përqind). Metali është paramagnetik (i tërhequr dobët nga një magnet). Ekziston në dy forma: kub me në qendër trupin (alfa) dhe gjashtëkëndore e mbyllur (beta). Në temperaturën e dhomës, kromi tretet ngadalë në acide klorhidrike dhe të holluara. Disa agjentë oksidues prodhojnë një shtresë të hollë oksidi joreaktiv në metal, duke e bërë atë pasiv edhe për të holluar acidet minerale, të tilla si sulfurik, nitrik ose aqua regia (ujë mbretëror) e ftohtë. Në temperatura të zakonshme metali nuk tregon asnjë reagim ndaj ujit të detit ose ajrit të lagësht ose të thatë.
Prodhuesit kryesorë të kromit përfshijnë Afrikën e Jugut, Indinë, Kazakistanin dhe Turqinë.
Komponimet kryesore
Gjendjet më të zakonshme të oksidimit të kromit janë +6, +3 dhe +2. Megjithatë, dihen disa përbërës të qëndrueshëm të gjendjeve +5, +4 dhe +1.
Në gjendjen e oksidimit +6, speciet më të rëndësishme të formuara nga kromi janë kromati, CrO42−, dhe dikromat, Cr2O72−, jonet. Këto jone formojnë bazën për një sërë kripërash të rëndësishme industrialisht. Midis tyre janë kromati i natriumit, Na2CrO4, dhe dikromat natriumi, Na2Cr2O7, të cilat përdoren në rrezitjen e lëkurës, në trajtimin e sipërfaqes së metaleve dhe si katalizatorë në procese të ndryshme industriale.
Kromi formon disa komponime oksigjeni me vlerë komerciale, më i rëndësishmi prej të cilëve është oksidi i kromit, i quajtur zakonisht trioksid kromi ose acid kromik, CrO3, në të cilën kromi është në gjendjen e oksidimit +6. Një acid kristalor portokalli-kuq, acidi kromik lëngësohet gradualisht kur ekspozohet ndaj ajrit të lagësht. Zakonisht prodhohet nga trajtimi i dikromatit të natriumit me acid sulfurik. Acidi kromik përdoret kryesisht për krom, por përdoret gjithashtu si ngjyrues në qeramikë. Është një oksidant i fuqishëm dhe mund të reagojë dhunshëm me disa materiale organike, por zgjidhje të tilla shpesh përdoren nga oksidime të kontrolluara në sintezën organike.]
Pyetjet e bëra më shpesh – FAQ (3)
Pyetja 1
Për çfarë përdoret elementi i kromit?
Kromi dhe lidhjet e tjera përdoren në çelik inox. Për shembull, në makina dhe biçikleta, kromi krijon një përfundim të lëmuar, argjendi që është shumë rezistent ndaj korrozionit. Metali përdoret zakonisht edhe si katalizator. Komponimet e kromit vlerësohen për ngjyrat e tyre të ndezura të jeshile, vjollcës, të kuqes dhe portokalli si pigmente.
Pyetja 2
Cilës familje i përket kromi?
Në Tabelën Periodike të Elementeve, kromi është një metal tranzicioni në Grupin 6. Kromi, në formën e tij të pastër, është një metal i fortë argjendi, me shkëlqim, me një përfundim të madh që është i përshtatshëm për galvanizim.
Pyetja 3
A është kromi toksik për njerëzit?
Rreziqet shëndetësore që lidhen me ekspozimin ndaj kromit bazohen në gjendjen e oksidimit të tij. Forma e metalit (kromi siç shfaqet në këtë produkt) ka një nivel të ulët toksiciteti. Forma gjashtëvalente është helmuese. Ulçerat, dermatiti dhe reaksionet alergjike të lëkurës mund të përfshijnë efekte negative të formës gjashtëvalente në lëkurë.
Pyetja 4
Cilat sëmundje mund të shkaktohen nga kromi?
Nëpërmjet inhalimit dhe rrugës së lëkurës, kromi është jashtëzakonisht toksik dhe shkakton kancer të mushkërive, inflamacion të hundës, ulçerë hundësh dhe reaksione të mbindjeshmërisë si dermatiti kontakti dhe astma. Kromi ka një efekt në aspekte të ndryshme të sistemit imunitar që mund të kontribuojë në imunostimulimin ose imunosupresionin.
Pyetja 5
Në cilat komponime të zakonshme gjendet kromi?
Kromati i natriumit, kromati i kaliumit, dikromati i kaliumit, dikromati i amonit dhe trioksidi i kromit janë komponime kromi gjashtëvalente që prodhohen gjerësisht.
–
Referencat