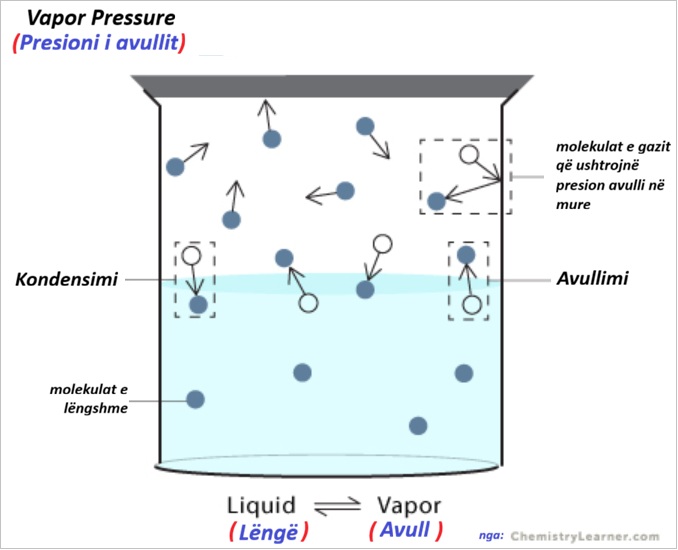
Presioni i avullit është presioni i ushtruar nga një gaz kur është në ekuilibër me formën e tij të lëngshme ose të ngurtë. Në një enë të mbyllur, disa molekula të një lëngu ikin gjithmonë në ajër si gaz, ndërsa disa molekula gazi kthehen në lëng. Kur numri i molekulave që largohen nga lëngu është i barabartë me numrin që kthehet, sistemi është në ekuilibër dhe presioni i avullit mbetet konstant.
Formula e presionit të avullit
Nga: Chemistry Learner> Vapor Pressure: Definition, Formula, Examples, and Table (1)
Presioni i avullit mund të llogaritet duke përdorur formula të ndryshme në varësi të situatës. Kjo varet nga temperatura dhe natyra e lëngut. Dy ekuacione të rëndësishme ndihmojnë në përshkrimin e presionit të avullit: Ligji i Raoulit dhe ekuacioni Clausius-Clapeyron.
Ligji i Raoulit
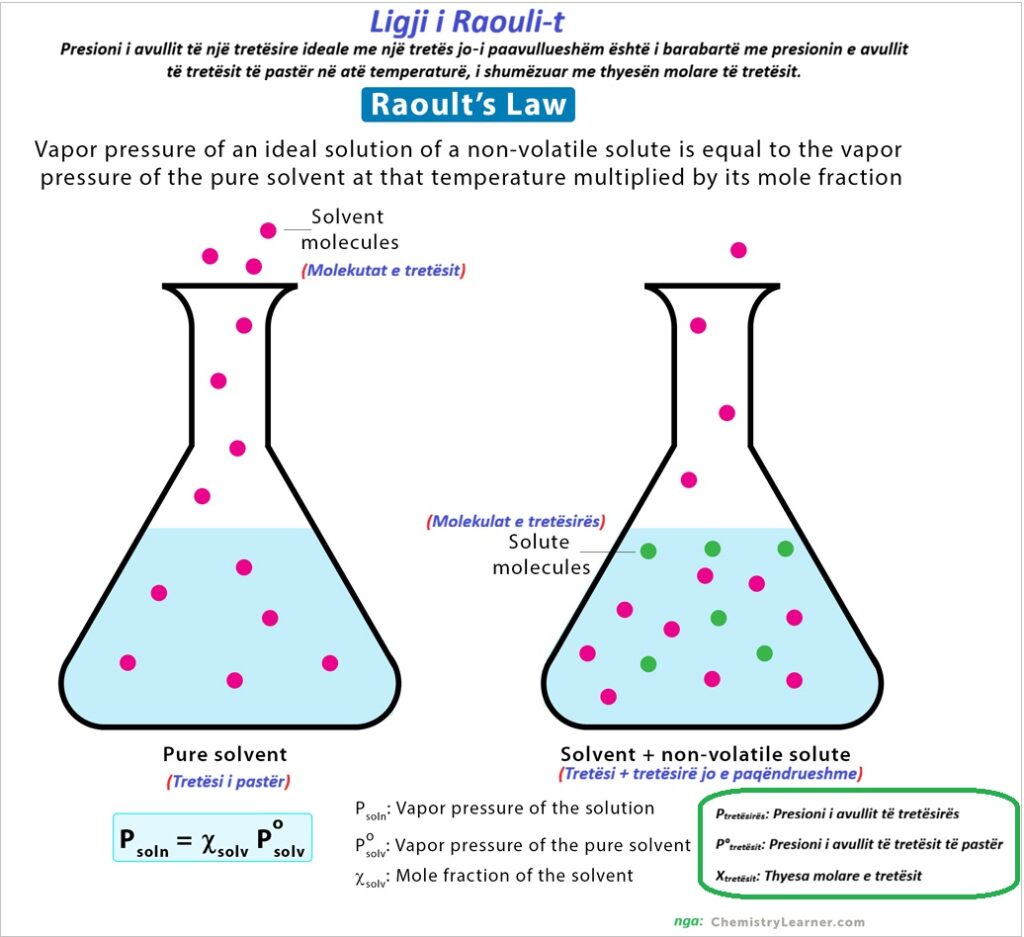
Ligji i Raoulit përshkruan se si shtimi i një lënde të tretur (si kripa ose sheqeri) në një lëng ul presionin e tij të avullit. Ligji thotë se presioni i avullit të një tretësire (Psoln) është më i ulët se ai i tretësit të pastër (Psolv) dhe varet nga fraksioni mol (Χsolv) të tretësit:
Psoln = Χsolv Psolv
Përkufizime:
Ptretësirës = Χtretësit P°tretësit
- Ptretësirës: Presioni i avullit të tretësirës
- P°tretësit: Presioni i avullit të tretësit të pastër
- Xtretësit: Thyesa molare e tretësit
Kjo do të thotë që kur një lëndë e tretur jo e paqëndrueshme (ajo që nuk avullon) shtohet në një lëng, më pak molekula mund të dalin në fazën e gazit, duke ulur presionin e avullit. Kjo është arsyeja pse uji i kripur avullon më ngadalë se uji i pastër.
Ligji i Raouli-t – ilustrim1a
Ndërsa Ligji i Raoult shpjegon efektin e lëndëve të tretura, ekuacioni Clausius-Clapeyron përshkruan se si temperatura ndikon në presionin e avullit.
Ekuacioni Clausius-Clapeyron
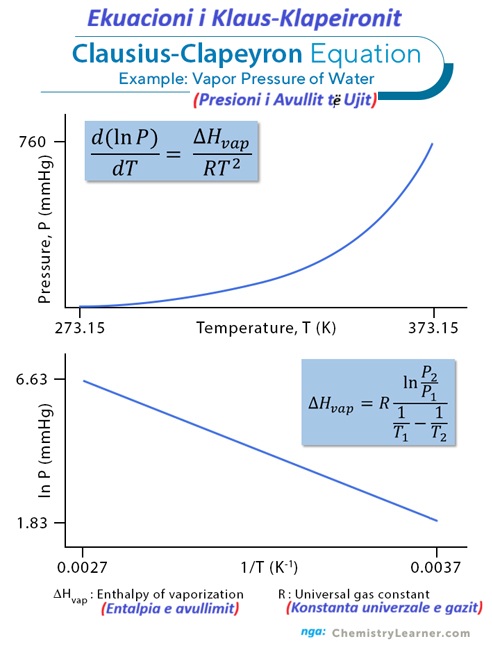
Ekuacioni Clausius-Clapeyron tregon se si presioni i avullit të një substance rritet me temperaturën. Është shkruar si:
ln (P2/P1) = (ΔHvap /R)(1/T1 – 1/T2
Ku:
- – P1: Presioni i avullit në temperaturën T1
- – P2: Presioni i avullit në temperaturën T2
- – ΔHVAP: Entalpia molare (nxehtësia) e avullimit
- – R: Konstante universale e gazit
- – T: Temperatura absolute në Kelvin
Ky ekuacion shpjegon pse lëngjet avullojnë më shpejt në temperatura më të larta. Ndërsa temperatura rritet, molekulat fitojnë më shumë energji për të dalë në fazën e gazit, duke rritur presionin e avullit. Për shembull, uji avullon më shpejt në një ditë të nxehtë sesa në një ditë të ftohtë sepse presioni i tij i avullit është më i lartë.
Ekuacioni i Klaus-Klapeironit – Presioni i Avullit të Ujit – ilustrim1a
–
Faktorët që ndikojnë në presionin e avullit
Dy faktorë kryesorë ndikojnë në presionin e avullit: natyra e lëngut dhe temperatura.
1. Natyra e lëngut
Lëngje të ndryshme kanë presione të ndryshme avulli në varësi të forcës së forcave të tyre ndërmolekulare. Nëse forcat e forta mbajnë së bashku molekulat në një lëng, ato e kanë më të vështirë të ikin në ajër, duke çuar në një presion më të ulët të avullit. Nga ana tjetër, nëse forcat midis molekulave janë të dobëta, ato shpëtojnë më lehtë, duke rezultuar në një presion më të lartë të avullit.
Për shembull, uji ka lidhje të forta hidrogjeni midis molekulave të tij, kështu që ka një presion më të ulët të avullit dhe avullon më ngadalë. Në të kundërt, acetoni (që gjendet në heqësin e manikyrit) ka forca më të dobëta midis molekulave të tij, duke e lejuar atë të avullojë shpejt dhe të ketë një presion më të lartë të avullit. Kjo është arsyeja pse acetoni thahet shumë më shpejt se uji kur lihet në një enë të hapur.
2. Temperatura
Temperatura ka një efekt të drejtpërdrejtë në presionin e avullit. Ndërsa temperatura rritet, molekulat në një lëng fitojnë më shumë energji kinetike dhe lëvizin më shpejt. Kjo lejon që më shumë molekula të dalin në fazën e gazit, duke rritur presionin e avullit.
Një shembull i thjeshtë është uji i vluar. Në temperaturën e dhomës, uji ka një presion relativisht të ulët të avullit, por kur nxehet, presioni i avullit rritet. Uji vlon kur presioni i tij i avullit është i barabartë me presionin atmosferik përreth. Kjo është arsyeja pse uji vlon në 100°C në nivelin e detit, por në një temperaturë më të ulët në vendet në lartësi të mëdha ku presioni atmosferik është më i ulët.
Një grafik i presionit të avullit kundrejt temperaturës tregon një kurbë të pjerrët që rritet me rritjen e temperaturës. Kjo do të thotë se edhe një rritje e vogël e temperaturës mund të shkaktojë një rritje të madhe të presionit të avullit, prandaj lëngjet avullojnë më shpejt në ditët e nxehta.
Njësitë e presionit të avullit
Presioni i avullit matet në njësi të ndryshme në varësi të kontekstit. Njësitë më të përdorura janë:[1-5]
- Pascal (Pa): Njësia SI e presionit, ku 1 Pa = 1 N/m².
- Torr (ose mmHg): Përdoret zakonisht në kimi, ku 1 Torr = 1 mmHg (milimetër merkur). Presioni standard atmosferik është 760 Torr.
- Atmosfera (atm): Përdoret në matjet e përgjithshme të presionit, ku 1 atm = 101.325 kPa = 760 mmHg.
- Bar: Një njësi tjetër e përdorur në fizikë dhe inxhinieri, ku 1 bar = 100 kPa.
Për shembull, presioni i avullit të ujit në 25 °C është 23.8 mmHg ose 0.0313 atm ose 23.8 torr ose 3.17 kPa.
Tabela e presionit të avullit
| Substanca | Presioni i avullit në 25 °C (atm) |
| Eter dietil | 0.7 |
| Bromi | 0.3 |
| Alkooli etilik | 0.08 |
| Ujë | 0.03 |
Shembuj të presionit të avullit
- Uji i vluar: Në nivelin e detit, uji vlon në 100°C sepse presioni atmosferik është i lartë. Në zonat me lartësi të mëdha, si malet, presioni atmosferik është më i ulët, kështu që uji vlon në një temperaturë më të ulët.
- Alkooli i fërkimit: Kur aplikoni alkool fërkimi në lëkurë, ai avullon shpejt dhe e bën lëkurën tuaj të ndihet e freskët. Kjo ndodh sepse alkooli ka një presion më të lartë të avullit se uji, që do të thotë se kthehet në gaz më lehtë.
- Difuzioni i parfumit: Kur spërkatni parfumin, ai avullon shpejt sepse përmban lëngje të paqëndrueshme me presion të lartë të avullit. Kjo lejon që aroma të përhapet në ajër.
- Avullimi i benzinës: Benzina ka një presion të lartë avulli, i cili e lejon lehtësisht atë të avullojë kur ekspozohet ndaj ajrit. Kjo është arsyeja pse shpesh nuhasni tymrat e benzinës pranë një pike karburanti ose kur furnizoni një makinë.
–
Referencat