Galiumi është një element kimik me numër atomik 31 dhe simbol të elementit Ga. Konsiderohet të jetë një metal pas tranzicionit ose metal bazë. Galiumi është i njohur për pikën e tij të ulët të shkrirjes, e cila i jep vetes demonstrimin e lugës së galiumit dhe madje edhe shkrirjen e metalit të pastër në dorën tuaj. Këtu është një koleksion i fakteve të galiumit, duke përfshirë zbulimin, vetitë, përdorimet dhe burimet e elementit.
Faktet bazë të galiumit (1)
Emri i elementit: Gallium
Numri atomik: 31
Simboli i elementit: Ga
Masa atomike: 69.723(1)
Grupi: Grupi 13 ose grupi i borit
Periudha: Periudha 4
Blloku: bllok p
Familja e elementeve: Metal pas tranzicionit ose metal bazë
Pamja: Në temperaturën e dhomës, galiumi është një metal i ngurtë i butë, blu argjendi.
Konfigurimi i elektroneve: [Ar] 3d10 4 s2 4p1
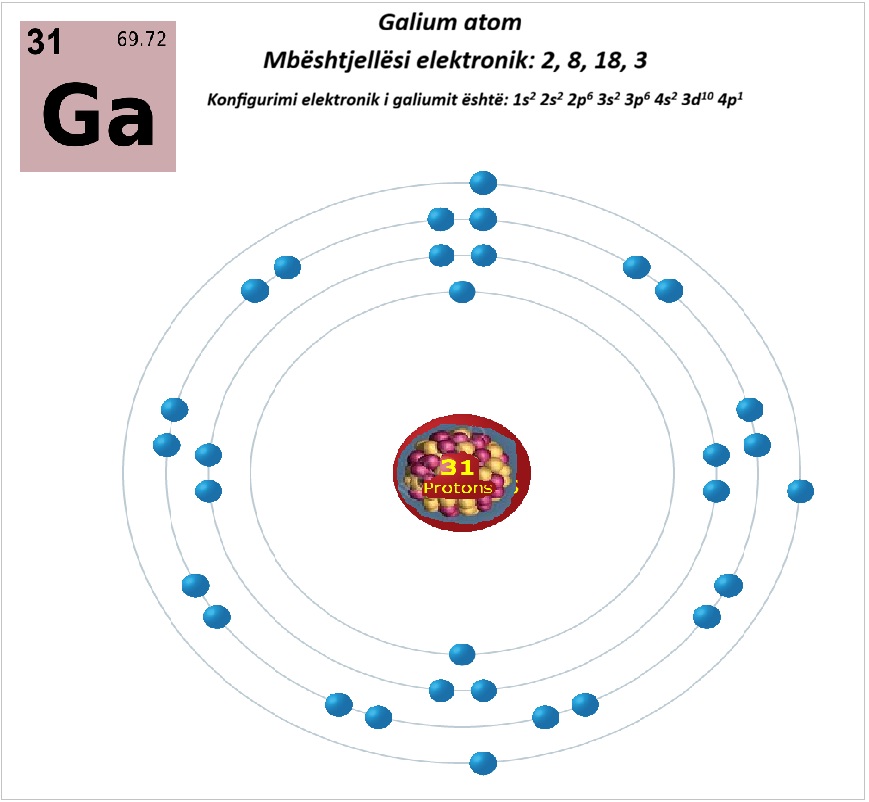
Galium atom ilustrim1a. – Konfigurimi i elektroneve të atomit të galiumit.
Konfigurimi elektronik i galiumit është: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p1
Zbulimi: Lecoq de Boisbaudran zbuloi dhe izoloi galiumin në 1875. Megjithatë, Dmitri Mendeleev parashikoi ekzistencën e elementit në 1871. Mendeleev e quajti elementin e propozuar “eka-aluminium” nga pozicioni i tij në tabelën periodike. Lecoq de Boisbaudran identifikoi galiumin nga dy linja spektrale vjollcë në një mostër sfaleriti. Ai e izoloi elementin duke përdorur elektrolizën e hidroksidit.
Origjina e fjalës: de Boisbaudran e quajti elementin 31 “gallia” për të nderuar vendlindjen e tij, Francën. Gallia është emri latin për Galinë. Disa thonë gjithashtu se emri i de Boisbaudran ishte një lojë fjalësh, duke e emërtuar elementin për veten dhe Francën. “Le coq” është fjala frënge për “gjeli”, ndërsa fjala latine për “gjeli është “gallus”. Elementi më vonë u quajt galium në përputhje me prapashtesën -ium për elementet metalike.
Izotopet: 31 izotopet e njohura të galiumit variojnë nga numri i masës 56 në 86. Dy izotope janë të qëndrueshme dhe ndodhin në natyrë: galium-69 dhe galium-71. Galiumi-69 përbën 60.1% të bollëkut natyror, ndërsa galiumi-71 përbën 39.9%. Të gjitha izotopet e tjera janë radioaktive.
Përdorimet: Galiumi përdoret për të bërë termometra, veçanërisht duke zëvendësuar merkurin toksik. Galiumi është i rëndësishëm për të prodhuar pajisje në gjendje të ngurtë dhe gjysmëpërçues drogë. Arsenidi i galiumit konverton energjinë elektrike në dritë koherente. Metali formon një shtresë të shkëlqyer pasqyre. Zemra që rreh galiumit është një alternativë më e sigurt për demonstrimin e zemrës që rreh merkurin.
Roli biologjik: Galiumi nuk shërben asnjë rol në biologjinë e njeriut, kafshëve ose bimëve. Metali i pastër konsiderohet jo toksik. Megjithatë, galiumi zëvendëson hekurin (III) në trup. Në baktere, të tilla si Pseudomonas, marrja e galiumit mund të ndërhyjë në frymëmarrje dhe të çojë në vdekjen e qelizave. Në mjekësinë njerëzore, galiumi përdoret për të gjurmuar inflamacionin dhe për të shënuar tumoret. Elementi ka veti antikancerogjene, veçanërisht kundër limfomës jo-Hodgkin dhe kancerit urotelial. Një përbërës aminë-fenol galium është toksik për parazitët e malarias, duke përfshirë ata rezistent ndaj klorokinës.
Burimet: Burimi kryesor komercial i galiumit është minerali i boksitit. Prodhimi i galiumit është një nënprodukt i përpunimit të aluminit. Sasi më të vogla të galiumit nxirren nga sfaleriti, minerale të tjera sulfuri zinku dhe disa lloje qymyri. Izolimi i galiumit ndodh me elektrolizë të hidroksidit të tij në tretësirën e hidroksidit të kaliumit.
Të dhënat fizike
Dendësia: 5.91 g/cm3
Pika e shkrirjes: 302.9146 K (29.7646 °C, 85.5763 °F)
Pika e vlimit: 2673 K (2400 °C, 4352 °F)
Gjendet në 20ºC: E ngurtë
Nxehtësia e shkrirjes: 5.59 kJ/mol
Nxehtësia e avullimit: 256 kJ/mol
Kapaciteti i nxehtësisë molare: 25.86 J/(mol· K)
Renditja magnetike: Diamagnetike
Struktura kristalore: Ortorombike
Fortësia Mohs: 1.5
Të dhënat atomike
Rrezja atomike: 135 pm (empirike)
Rrezja kovalente: 122±3 pm
Rrezja e Van der Waals: 187 pm
Elektronegativiteti: 1.81 (shkalla Pauling)
Energjia e jonizimit të 1-të: 578.8 kJ/mol
Energjia e 2-të e jonizimit: 1979.3 kJ/mol
Energjia e jonizimit të 3-të: 2963 kJ/mol
Gjendjet e oksidimit: -5, -4, -2, -1, +1, +2, +3
10 fakte të galiumit

- Galliumi elementar nuk ndodh i lirë në natyrë. Megjithatë, shkrirja lëshon lehtësisht metalin.
- Mund të shkrini galiumin në pëllëmbën e dorës ose të bëni një lugë prej tij që do të shkrihet në një pije të nxehtë.
- Nga të gjithë elementët, galiumi ka diapazonin më të lartë të temperaturës si lëng. Ka 2373 °C midis pikës së shkrirjes së galiumit dhe pikës së vlimit!
- Ndryshe nga shumica e substancave, galiumi zgjerohet kur ngrin. Një material tjetër që shfaq këtë sjellje është uji. Galiumi nuk duhet të ruhet në enë qelqi ose metalike sepse ato mund të copëtohen kur elementi ngurtësohet.
- Arsenidi i galiumit përdoret për të prodhuar LED blu jashtëzakonisht të ndritshme.
- Galliumi i lëngshëm formon një pasqyrë të jashtëzakonshme sepse elementi lag shumë sipërfaqe. Galiumi lag qelqin, porcelanin dhe madje edhe lëkurën e njeriut.
- “Zemra që rreh galiumin” është një zëvendësues i sigurt për demonstrimin e kimisë “zemra që rreh merkur”.
- Mbi 95% e galiumit përdoret në industrinë e gjysmëpërçuesve.
- Galliumi i pastër i reziston sulmit nga acidet minerale. Shtresa e oksidit që formohet në sipërfaqe mbron brendësinë.
- Kur shtohet në metale të tjera, galiumi formon lidhje me shkrirje të ulët.
Referencat
- Greenwood, N. N.; Earnshaw, A. (1997). Kimia e elementeve (botimi i 2-të). Oksford: Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Lehto, RS (1968). “Zinku”. Në Clifford A. Hampel. Enciklopedia e elementeve kimike. Nju Jork: Korporata e Librit Reinhold. fq. 822–830. ISBN 0-442-15598-0.
- Lide, David R., ed. (2006) Manuali i Kimisë dhe Fizikës (botimi i 87-të). Boca Raton, Florida: CRC Press, Taylor & Francis Group. ISBN 0-8493-0487-3.
- Nordberg, Gunnar F.; Fowler, Bruce A.; Nordberg, Monica (2014). Manuali mbi Toksikologjinë e Metaleve
–
Burimi>



