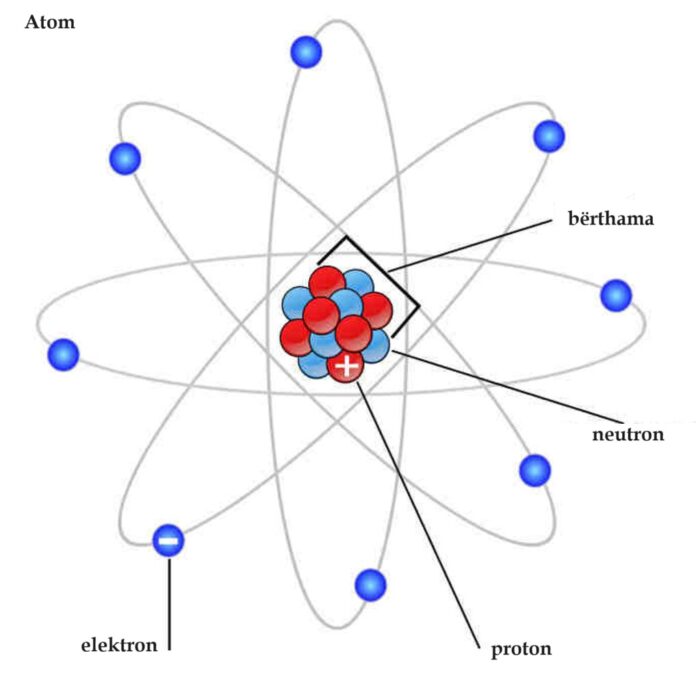
Një atom është njësia më e vogël e materies në univers që formon një element natyror (element kimik). Çdo atom i ngurtë, i lëngshëm, gaz dhe plazmë përbëhet nga atome neutrale ose të jonizuara.
Një atom përbëhet nga një bërthamë me protone dhe neutrone që është e rrethuar nga elektronet.
Një atom është pjesa më e vogël e një elementi dhe përbëhet nga protone, neutrone dhe elektrone. E gjithë materia përbëhet nga grimca të vogla të quajtura atome.
Protonet, të cilët janë të ngarkuar pozitivisht dhe neutronet, të cilët janë neutralë, rrinë së bashku në qendër të atomit për të formuar bërthamën. Rreth bërthamës sillen dhe rrotullohen elektronet, grimca të ngarkuara negativisht, që formoin orbita të elektroneve, që formoin mbështjellësin elektronik, pak si planetët që rrotullohen rreth Diellit. Këto elektrone janë të vendosura në shtresa si shtresat një mbi një, si fletët në një qepe. Këto shtresa quhen guaskë elektronike. Më shumë se 99.9% e një atomi është hapësirë boshe e zënë nga elektronet.
Atomet janë grimca të vockla që formojnë blloqet bazë të ndërtimit të të gjitha materieve në univers, qofshin ato të ngurta, të lëngshme ose të gazit. Të gjithë organizmat e gjallë dhe objektet që jetojnë në Tokë por edhe në kosmos janë bërë nga triliona dhe triliona atome.
Grimcat më të vogla që përbëjnë një atom njihen si grimca subatomike.
–
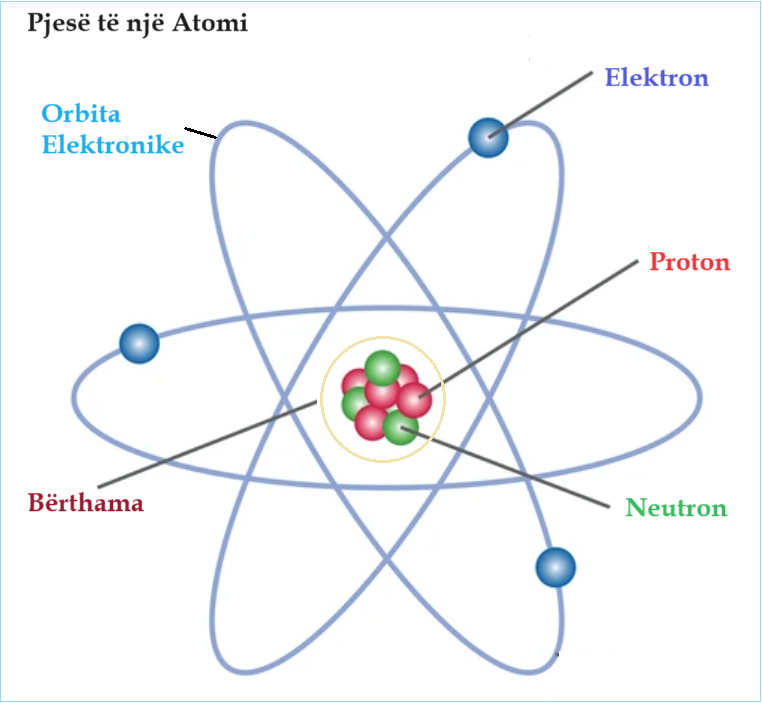
Imazhi: Pjesë të një Atomi
Termi ‘atom’ rrjedh nga fjala greke ‘atomos’, që do të thotë ‘i pandashëm’.
Filozofët e lashtë grekë dhe indianë ishin të parët që menduan atomin si njësinë bazë të të gjitha materieve në univers.
Në fillim të 19th shekulli, shkencëtarët filluan të kuptonin strukturën e atomit me pjesët e tyre të brendshme më hollësisht. Në vitin 1926, Erwin Schrodinger propozoi modelin atomik aktual që ne përdorim ende sot.
Ka shumë atome të ndryshme, secili ka emrin, madhësinë, masën dhe numrin e grimcave subatomike. Ato njihen si elemente. Kështu, një atom mund të përkufizohet edhe si njësia strukturore më e thjeshtë e një elementi që ruan të gjitha vetitë e tij. Sot ekzistojnë 94 elemente natyrore dhe 24 elemente artificiale.
Madhësia e një atomi
Madhësia e një atomi është e vogël, me një diametër prej 0.1 deri në 0.5 nanometra (1 × 10−10 është 5 × 10−10 m). Kështu, ata nuk mund të shihen me syrin tonë të zhveshur.
Madhësia e një atomi është shumë e vogël, rreth 0.1 nm ose 100 pm. Megjithatë, madhësia e saktë e një atomi është e vështirë të matet sepse elektronet që rrethojnë bërthamën nuk janë të fiksuara në një vend. Një mënyrë për të vlerësuar madhësinë e një atomi është të supozojmë se ajo është gjysma e distancës midis atomeve ngjitur në një solid. Bërthama e një atomi është shumë më e vogël se vetë atomi, më pak se 1/10,000 e rrezes së atomit. Një shtresë e një atomi është disi e ngjashme me një fletë letre.
Struktura atomike
Të gjitha atomet përveç hidrogjenit përmbajnë tre grimca subatomike bazë:
1) elektronet, 2) protonet dhe neutronet.
Neutronet dhe protonet gjenden në qendër të atomit brenda një rajoni të dendur të quajtur bërthama. Në kontrast, elektronet gjenden jashtë bërthamës në një rajon të quajtur rea elektronike ose guaska elektronike.
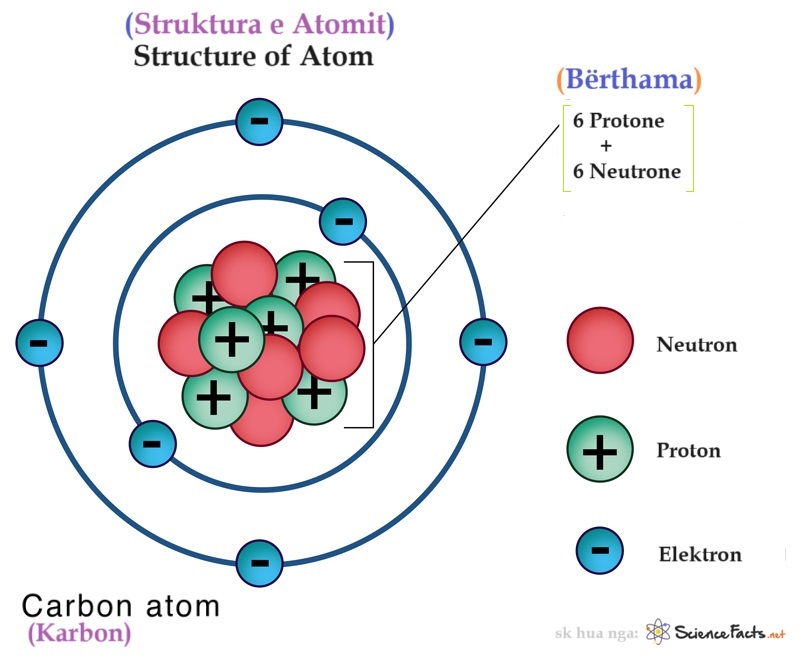
-Imazhi> Struktura e Atomit me pjesë.
1) Elektronet
Ato janë grimca të ngarkuara negativisht që rrotullohen rreth bërthamës në një orbitë fikse. Ndryshe nga protonet dhe neutronet, elektronet janë grimca themelore shumë më të vogla, pothuajse 1800 herë, në madhësi se protonet dhe neutronet. Simboli standard që përdoret për një elektron është e ose e–. Fizikani britanik J.J. Thomson e zbuloi atë në vitin 1897.
Elektronet lëvizin kaq shpejt rreth bërthamës, saqë vendndodhja e tyre e saktë brenda një atomi nuk mund të përcaktohet me saktësi. Kur numri i elektroneve të ngarkuara negativisht është i barabartë me numrin e protoneve të ngarkuara pozitivisht, atomi është neutral në ngarkim.
2) Protonet
Protonet janë grimca të ngarkuara pozitivisht që gjenden brenda një rajoni të dendur në qendër të atomit të quajtur bërthama (nukleusi). Ato u zbuluan nga Ernest Rutherford në vitin 1917 dhe janë shënuar nga simboli p ose p+. Protonet përbëhen nga grimca edhe më të vogla të quajtura quarks dhe gluons.
Të ngjeshura fort me bërthamën (nukleus), ato përbëjnë pothuajse të gjithë masën e një atomi, së bashku me neutronet.
3) Neutronet
Ato gjenden edhe brenda bërthamës së bashku me protonet në një mënyrë të ngjeshur fort. Neutronet, të ngjashme me protonet, janë bërë nga kuarqet dhe gluonet (quarks dhe gluons). Ato u zbuluan nga James Chadwick në vitin 1932 dhe janë shënuar nga simboli n ose n0.
Neutronet janë grimca neutrale pa ngarkesë, por kanë një madhësi dhe masë të konsiderueshme të ngjashme me një proton.Më poshtë është një tabelë që tregon ngarkesën, masën dhe vendndodhjen e tre grimcave nën-atomike:
| Emri i thërrmijës | Simboli Ngarkesa relative | Ngarkesa relative | Vendndodhja në Atom |
| 1. Proton | p/p+ | +1 | Bërthama |
| 2. Neutron | n/n0 | 0 | Bërthama |
| 3. Elektron | e/g– | -1 | Orbit (Mbështjellës) |
Grimca të tjera themelore
Kuarqet (Quarks): Ato janë grimca subatomike themelore që përbëjnë protonet dhe neutronet. Ato u zbuluan në mënyrë të pavarur nga Murray Gell-Mann dhe George Zweig në vitin 1964. Megjithatë, pozicioni i tyre i saktë në një atom nuk mund të matet me saktësi. Kuarqet (Quarks) janë të gjashtë llojeve të ndryshme: lart, poshtë, sipër, fundi, sharm dheçuditshëm. Një proton përmban tre kuarqe (dy kuarqe lart dhe një poshtë kuark), ndërsa një neutron përmban (dy kuarqe poshtë dhe një lart kuark).
Gluone (Gluons): Gjithashtu gjenden brenda protoneve dhe elektroneve, ato veprojnë si grimca shkëmbimi që ndihmojnë në transferimin e forcës së fortë midis kuarqeve. John Ellis dhe kolegët e tij të punës i zbuluan ato në vitin 1979.
Neutrino: Ato janë të ngjashme me elektronet e formuara nga reaksionet bërthamore. Neutrino nuk ka ngarkesë por udhëton me një shpejtësi shumë të lartë, të ngjashme me shpejtësinë e dritës, dhe mund të kalojë nëpër çdo objekt të ngurtë. Energjia e jashtëzakonshme e diellit, e cila përftohet nga bashkimi bërthamor, çliron triliona neutrino çdo sekondë.
Leptonet. Përkufizimi: Një lepton si elektroni, muoni dhe tauoni është një grimcë elementare me spin gjysmë të plotë (spin = 1/2) që nuk i nënshtrohet ndërveprimeve të forta. Ndryshe nga kuarkët, të cilët i nënshtrohen forcës së fortë, leptonët mbeten të paprekur prej saj. Leptonet e ngarkuar mund të kombinohen me grimca të tjera për të formuar struktura të përbëra si atomet dhe pozitronet.
Karakteristikat e Atomit
Idetë e shkencëtarëve rreth atomeve kanë ndryshuar me kalimin e kohës. Sot, ata janë dakord se atomet kanë një bërthamë të ngarkuar pozitivisht të bërë nga protonet dhe neutronet, dhe elektronet e ngarkuara negativisht që rrotullohen rreth bërthamës në guaska mbështjellëse.
Atomi, blloku bazë i ndërtimit të të gjitha materieve dhe kimisë. Atomet mund të kombinohen me atome të tjera për të formuar molekula, por nuk mund të ndahen në pjesë më të vogla nga proceset e zakonshme kimike.
Në një atom të çdo elementi të veçantë, ka gjithmonë të njëjtin numër elektronesh dhe protonesh. Është numri i protoneve që i jep elementit numrin e tij atomik. Kështu, për shembull, një atom karboni ka gjashtë protone në bërthamën e tij, ka gjashtë elektrone që e rrethojnë dhe ka një numër atomik prej gjashtë. Elementi është gjithashtu neutral elektrik pasi numri i protoneve të ngarkuar pozitivisht dhe elektroneve të ngarkuar negativisht janë të njëjta (neutroni është i ngarkuar neutralisht, kështu që nuk ndikon në ngarkesën elektrike të atomit). Të gjithë atomet e një elementi kanë të njëjtin numër protonesh. Megjithatë, disa kanë numër të ndryshëm neutronesh. Këta quhen izotopë. Për shembull, atomet e karbonit zakonisht kanë gjashtë protone dhe gjashtë neutrone në bërthamat e tyre me një masë atomike prej 12. Megjithatë, nëse atomi ka tetë neutrone, ai do të ishte një izotop. Në këtë rast, do të quhej C-14, i cili është një izotop radioaktiv i karbonit. Atomet e elementeve të ndryshëm ndryshojnë, me masa dhe ngjyra të ndryshme. Atomet e një elementi mund të kombinohen me atomet e një tjetri për të formuar një substancë të re të quajtur një përbërje. Përbërjet mbahen së bashku me lidhje jonike, lidhje kovalente ose lidhje metalike. Grimcat më të mëdha në përbërje quhen molekula. Për shembull, kur dy atome hidrogjeni (H) bashkohen me një atom oksigjen (O) ne marrim përbërjen e ujit (H2O). Atomet gjithashtu mund të bashkohen në një përzierje ku atomet nuk janë të kombinuara kimikisht, por fizikisht.
–
Pjesa më e madhe e atomit është hapësirë boshe. Pjesa tjetër përbëhet nga tre lloje bazë të grimcave subatomike: protonet, neutronet dhe elektronet. Protonet dhe neutronet formojnë bërthamën qendrore të atomit. (Atomi i zakonshëm i hidrogjenit është një përjashtim; ai përmban një proton, por jo neutrone.) Siç sugjerojnë emrat e tyre, protonet kanë një ngarkesë elektrike pozitive, ndërsa neutronet janë elektrikisht neutrale—ato nuk mbajnë asnjë ngarkesë; Në përgjithësi, pra, bërthama ka një ngarkesë pozitive. Rreth bërthamës është një re elektronesh, të cilat janë të ngarkuara negativisht. Ashtu si skajet e kundërta të një magneti që tërheqin njëri-tjetrin, elektronet negative tërhiqen nga një forcë pozitive, e cila i lidh ato me bërthamën. Bërthama është e vogël dhe e dendur në krahasim me elektronet, të cilat janë grimcat më të lehta të ngarkuara në natyrë. Elektronet rrethojnë bërthamën në shtigjet orbitale të quajtura guaska, secila prej të cilave mban vetëm një numër të caktuar elektronesh.
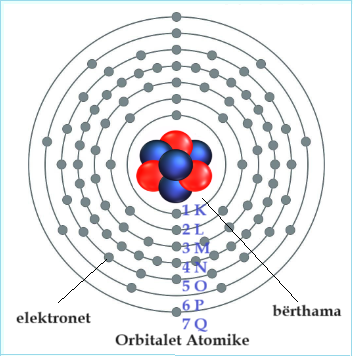
Imazhi: Orbitalet Atomike a1 orbitalet 1K 2L 3M 4N 5O 6P 7Q
Neutraliteti Atomit
Një atom i zakonshëm, neutral ka një numër të barabartë protonesh (në bërthamë) dhe elektrone (që rrethojnë bërthamën). Kështu ngarkesat pozitive dhe negative janë të balancuara. Disa atome, megjithatë, humbasin ose fitojnë elektrone në reaksione kimike ose në përplasje me grimca të tjera. Atomet e zakonshme që fitojnë ose humbasin elektronet quhen jone. Nëse një atom neutral humbet një elektron, ai bëhet një jon pozitiv. Nëse fiton një elektron, bëhet një jon negativ. Këto grimca subatomike bazë—protonet, neutronet dhe elektronet—janë vetë të përbëra nga substanca më të vogla, si kuarkët dhe leptonet.
Pytje të shpeshta
Sa atome ka në univers?
Ka afërsisht midis 1078 dhe 1082 Atomet e pranishme në univers.
Si lidhen atomet dhe elementet?
Një element është bërë tërësisht nga vetëm një lloj atomi. Me fjalë të tjera, një element është bërë nga atome të shumta që janë të të njëjtit lloj.
Si ndryshojnë molekulat nga atomet?
Një atom është njësia më e vogël e një elementi, ndërsa një molekulë përbëhet nga dy ose më shumë atome.
Çfarë ndodh kur një atom humbet një elektron?
Kur një atom humbet një elektron, ai bëhet një jon pozitiv.
Çfarë është një atom?
Një atom është blloku themelor i ndërtimit të kimisë. Është njësia më e vogël në të cilën materia mund të ndahet pa lëshuar grimca të ngarkuara elektrike. Është gjithashtu njësia më e vogël e materies që ka vetitë karakteristike të një elementi kimik.
A janë të gjithë atomet me të njëjtën madhësi?
Të gjithë atomet janë afërsisht të njëjtën madhësi, pavarësisht nëse kanë 3 ose 90 elektrone. Afërsisht 50 milionë atome të materies së ngurtë të rreshtuara me radhë do të mateshin 1 cm (0,4 inç). Një njësi e volitshme e gjatësisë për matjen e madhësive atomike është angstrom, e përcaktuar si 10−10 metra.
Nga çfarë përbëhet masa e një atomi?
Masa e një atomi përbëhet nga masa e bërthamës plus ajo e elektroneve. Kjo do të thotë se njësia e masës atomike nuk është tamam e njëjtë me masën e protonit ose neutronit.
Si përcaktohet numri atomik i një atomi?
Karakteristika e vetme më e rëndësishme e një atomi është numri atomik i tij (zakonisht i përmendur nga shkronja Z), i cili përkufizohet si numri i njësive të ngarkesës pozitive (protonet) në bërthamë. Për shembull, nëse një atom ka një Z prej 6, ai është karboni, ndërsa një Z prej 92 korrespondon me uraniumin.
-etj.
Referencat
Atom: Defhinition, Structure & Parts with Labeled Diagram (sciencefacts.net)
Atom | Definition, Structure, History, Examples, Diagram, & Facts | Britannica