Skandium, simboli Sc, është një element kimik, me numrin atomik 21. Është një element metalik i bardhë argjendi që gjendet në bllokun-d të tabelës periodike. Zakonisht, klasifikohet si një element i tokës së rrallë, së bashku me itriumin dhe lantanidet. Ajo u zbulua në 1879 nga analiza spektrale e mineraleve euxenite dhe gadolinite nga Skandinavia. Emri i elementit skandium rrjedh nga emri për Skandinavinë.
Prodhimi Skandiumit dhe Tregjet dhe përdorimet e skandiumit.
[: Skandiumi është i pranishëm në shumicën e depozitave të komponimeve të tokës së rrallë dhe uraniumit, por nxirret nga këto minerale në vetëm disa miniera në mbarë botën. Për shkak të disponueshmërisë së ulët dhe vështirësive në përgatitjen e skandiumit metalik, e cila u bë për herë të parë në 1937, aplikimet për skandium nuk u zhvilluan deri në vitet 1970, kur u zbuluan efektet pozitive të skandiumit në lidhjet e aluminit. Përdorimi i tij në lidhje të tilla mbetet aplikimi i tij i vetëm kryesor. Tregtia globale e oksidit të skandiumit është 15-20 tonë në vit.
Vetitë e komponimeve të skandiumit janë të ndërmjetme midis atyre të aluminit dhe itriumit. Ekziston një marrëdhënie diagonale midis sjelljes së magnezit dhe skandiumit, ashtu siç ekziston midis beriliumit dhe aluminit. Në komponimet kimike të elementeve në grupin 3, gjendja mbizotëruese e oksidimit është +3. (1)].
Vetitë tabelare të Skandium-it nga Wikipedia
| Skandium: 21Sc |
| Pamja: e bardhë e argjendtë |
Pesha standarde atomike Ar° (Sc): • 44.955907±0.000004, • 44.956±0.001 (shkurtuar) |
| Skandiumi në tabelën periodike |
| Numri atomik (Z): 21 |
| Grupi: Grupi 3 |
| Periudha: periudha 4 |
| Bllok: Blloku D |
| Konfigurimi i elektroneve: [Ar] 3d1 4s2 |
| Elektronet për guaskë: 2, 8, 9, 2 |
| Vetitë fizike |
| Faza në STP: Ngurtë (e fortë) |
| Pika e shkrirjes: 1814 K (1541 °C, 2806 °F) |
| Pika e shkrirjes: 1814 K (1541 °C, 2806 °F) |
| Pika e vlimit: 3109 K (2836 °C, 5136 °F) |
| Dendësia (në 20° C): 2.989 g/cm3, kur është i lëngshëm (në MP- pikë shkrirje): 2.80 g/cm3 |
| Nxehtësia e shkrirjes: 14.1 kJ/mol |
| Nxehtësia e avullimit: 332.7 kJ/mol |
| Kapaciteti i nxehtësisë molare: 25.52 J/(mol· K) |
| Kapaciteti specifik i nxehtësisë: 567.666 J/(kg· K) |
| Presioni i avullit: P (Pa): në T (K): 1 Pa në 1645 K 10 Pa në 1804 K 100 Pa në (2006 K) 1 mijë Pa në (2266 K) 10 mijë Pa në (2613 K) 100 mijë Pa në (3101 K) |
| Vetitë atomike |
| Gjendja e oksidimit: E zakonshme: +3, 0, +1, +2 |
| Elektronegativiteti, Shkalla Pauling: 1.36 |
| Energjitë e jonizimit: • 1: 633.1 kJ/mol, • 2: 1235.0 kJ/mol, • 3: 2388.6 kJ/mol, • (më shumë) |
| Rrezja kovalente: 170±7 pm |
| Rrezja e Van der Waals: 211 pm |
| Linjat spektrale të skandiumit: |
| Veti të tjera Ndodhia natyrore: Primordiale |
| Struktura kristalore: gjashtëkëndore e paketuar ngushtë (hcp) (hP2) |
Konstantet e grilës: 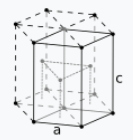 a = 330.89 pm c = 526.80 pm (në 20 °C) a = 330.89 pm c = 526.80 pm (në 20 °C) |
| Zgjerimi termik: 9.97×10−6/K (në 20 °C) |
| Përçueshmëria termike: 15.8 W/(m⋅K) |
| Rezistenca elektrike: α, poli: 562 nΩ⋅m (në rt, i llogaritur) |
| Porositja magnetike: paramagnetike |
| Ndjeshmëria magnetike molare: +315.0×10−6 cm3/mol (292 K) |
| Moduli i Young: 74.4 GPa |
| Moduli i prerjes: 29.1 GPa |
| Moduli me shumicë: 56.6 GPa |
| Raporti i Poisson (efektit Poisson, deformimi (zgjerimi ose tkurrja): 0.279 |
| Fortësia Brinell: 736–1200 MPa |
| Numri CAS: 7440-20-2 |
| Histori |
| Emërtimi: pas Skandinavisë |
| Parashikimi: Dmitri Mendeleev (1871) |
| Zbulimi: Lars Fredrik Nilson (1879) |
| Izolimi i parë W. Fischer, K. Brünger, H. Grieneisen (1937) |
| Izotopet e skandiumit: 43Sc, 44Sc, deri 48Sc |
Karakteristikat kimike
Scandium është një metal i butë me një pamje argjendi. Ajo zhvillon një ngjyrë pak të verdhë ose rozë kur oksidohet nga ajri. Është i ndjeshëm ndaj motit dhe tretet ngadalë në shumicën e acideve të holluara. Nuk tretet në një përzierje 1:1 të acidit nitrik (HNO3) dhe acidit hidrofluorik 48.0% (HF), ndoshta për shkak të formimit të një shtrese pasive të papërshkueshme. Kthesat e skandiumit ndizen në ajër me një flakë të verdhë të shkëlqyeshme për të formuar oksid skandiumi.
Histori (2)
Në 1869, Mendeleev vuri re se kishte një hendek në peshën atomike midis kalciumit (40) dhe titanit (48) dhe parashikoi se kishte një element të pazbuluar me peshë atomike të ndërmjetme. Ai parashikoi se oksidi i tij do të ishte X2O3. Ajo u zbulua si skandium në 1879, nga Lars Frederik Nilson i Universitetit të Uppsala, Suedi. Ai e nxori atë nga euxenite, një mineral kompleks që përmban tetë okside metalike. Ai tashmë kishte nxjerrë oksidin e erbiumit nga euxenit, dhe nga ky oksid ai mori oksid iterbiumi dhe më pas një oksid tjetër të një elementi më të lehtë, spektri atomik i të cilit tregonte se ishte një metal i panjohur. Ky ishte metali që Mendeleev kishte parashikuar dhe oksidi i tij ishte Sc2O3.

Mineral skandiumi – a1.
Vetië, Bollëku dhe Përdorimi i Skandiumit
nga: Scandium | Chemical Element, Properties, & Uses | Britannica(3)
Skandium (Sc), element kimik, një metal i tokës së rrallë i Grupit 3 të tabelës periodike. Scandium është një metal i bardhë argjendi, mesatarisht i butë. Është mjaft i qëndrueshëm në ajër, por ngadalë do të ndryshojë ngjyrën e tij nga e bardha e argjendtë në një pamje të verdhë për shkak të formimit të Sc2O3 oksid në sipërfaqe. Metali tretet ngadalë në acidtë holluar – përveç acidit fluorik (HF), në të cilin një shtresë mbrojtëse trifluoride parandalon reagimin e mëtejshëm. Skandiumi është paramagnetik nga 0 K (-273 °C, ose -460 °F) në pikën e shkrirjes së tij (1,541 °C, ose 2,806 °F). Bëhet superpërçues në -273.1 °C (-459.6 °F) në presione që tejkalojnë 186 kilobar.
Pasi kimisti rus Dmitry Ivanovich Mendeleyev4 në 1871 parashikoi ekzistencën e këtij elementi, duke e quajtur atë në mënyrë provizore ekaboron, kimisti suedez Lars Fredrik Nilson në 1879 zbuloi oksidin e tij, scandia, në mineralet e tokës së rrallë gadolinit dhe euksenit, dhe kimisti suedez Per Teodor Cleve më vonë në 1879 identifikoi skandiumin si hipotetik ekaboron. Skandiumi gjendet në përmasa të vogla, përgjithësisht më pak se 0.2 për qind, në shumë nga mineralet e rënda të lantanideve dhe në shumë xehe kallaj, urani dhe tungsteni. Thortveitite (një silikat skandiumi) është i vetmi mineral që përmban sasi të mëdha skandiumi, rreth 34 për qind, por për fat të keq ky mineral është mjaft i rrallë dhe nuk është një burim i rëndësishëm i skandiumit. Bollëku kozmik i skandiumit është relativisht i lartë. Edhe pse është vetëm elementi i 50-të më i bollshëm në Tokë (bollëku i tij është i ngjashëm me atë të beriliumit), ai është rreth elementi i 23-të më i bollshëm në Diell.
Bollëku
Në natyrë, skandiumi ekziston në formën e një izotopi të qëndrueshëm, skandium-45. Midis 25 izotopeve radioaktive (duke përjashtuar izomeret bërthamore) me masa që variojnë nga 36 në 61, më i qëndrueshëm është skandiumi-46 (gjysma e jetës prej 83.79 ditësh), dhe më pak i qëndrueshëm është skandiumi-39 (gjysma e jetës më pak se 300 nanosekonda).
Skandiumi ndahet nga tokat e tjera të rralla nga reshjet e sulfatit të kaliumit të patretshëm të skandiumit ose nga nxjerrja e tiocianatit të skandiumit nga eteri dietil. Vetë metali u përgatit për herë të parë në vitin 1938 nga elektroliza e klorureve të kaliumit, litiumit dhe skandiumit në një përzierje eutektike (d.m.th., një përzierje që ka pikën më të ulët të shkrirjes së mundshme me ata përbërës). Skandiumi tani prodhohet kryesisht si nënprodukt i nxjerrjes së uraniumit nga minerali davidit, i cili përmban rreth 0.02 për qind oksid skandiumi. Scandium ekziston në dy forma alotropike (strukturore). Faza α është gjashtëkëndore e mbushur ngushtë me a = 3.3088 Å dhe c = 5.2680 Å në temperaturën e dhomës. Faza β është kubike me në qendër trupin me një vlerësim a = 3.73 Å në 1,337 °C (2,439 °F).
Përdorimi
Vetëm disa përdorime të këtij metali të pazakontë tranzicioni janë zhvilluar, kryesisht për shkak të disponueshmërisë së kufizuar dhe kostos së lartë të skandiumit. Dendësia e tij e ulët dhe pika e lartë e shkrirjes sugjerojnë aplikime si një agjent aliazhues për metale të lehta për aplikime ushtarake dhe me performancë të lartë. Përdorimet kryesore të skandiumit janë si një aditiv aliazh për lidhjet me bazë alumini për mallra sportive dhe në llambat haloide metalike me intensitet të lartë. Kur aliazhohet me alilumb dhe lidhje me bazë alumini, skandiumi kufizon rritjen e drithërave në temperaturë të lartë.

Aliazh Skandiumi – imazh1.
Njohuri të besueshme për ata që duan të dinë më shumë
Kimia e skandiumit ka një ngjashmëri më të madhe me atë të elementëve të tjerë të tokës së rrallë të gjendjes së oksidimit +3 sesa me atë të aluminit ose titanit. Disa nga sjelljet e tij, megjithatë, janë atipike për tokat e rralla për shkak të rrezes së saj dukshëm më të vogël jonike (1.66 Å për numrin e koordinimit 12) në krahasim me mesataren e tokës së rrallë (1.82 Å për numrin e koordinimit 12). Për këtë arsye, Sc3+ joni është një acid relativisht i fortë dhe ka një tendencë shumë më të madhe për të formuar jone komplekse.
Roli biologjik: Skandiumi nuk ka rol biologjik të njohur. Është një kancerogjen i dyshuar.
–
Referencat



