Germanium, është element kimik, me simbol Ge, numri atomik 32, në tabelën periodike gjendet në periudhën 4, grupi 14 (Grupi i Karbonit), blloku-p. Germaniumi është me shkëlqim, i fortë-i brishtë, gri-bardhë dhe i ngjashëm në pamje me silikonin. Është një metaloid (ndonjëherë konsiderohet jometal) në grupin e karbonit që është kimikisht i ngjashëm me silicin. Ashtu si silici, germaniumi reagon natyrshëm dhe formon komplekse me oksigjenin në natyrë.
[: Për shkak se rrallë shfaqet në përqendrim të lartë, germaniumi u gjet relativisht vonë në zbulimin e elementeve. Germaniumi renditet i 50-ti në bollëkun e elementeve në koren e Tokës. Në 1869, Dmitri Mendeleev parashikoi ekzistencën e tij dhe disa nga vetitë e tij nga pozicioni i tij në tabelën e tij periodike dhe e quajti elementin ekasilicon. Më 6 shkurt 1886, Clemens Winkler në Universitetin Freiberg gjeti elementin e ri, së bashku me argjendin dhe squfurin, në argiroditin mineral. Winkler e quajti elementin sipas Gjermanisë, vendit të tij të lindjes. Germaniumi nxirret kryesisht nga sfaleriti (minerali kryesor i zinkut), megjithëse germaniumi rikuperohet gjithashtu komercialisht nga mineralet e argjendit, plumbi dhe bakrit.
Germaniumi elementar përdoret si gjysmëpërçues në tranzistorë dhe pajisje të tjera elektronike të ndryshme. Historikisht, dekada e parë e elektronikës gjysmëpërçuese bazohej tërësisht në germanium. Aktualisht, përdorimet kryesore përfundimtare janë sistemet me fibra optike, optika infra të kuqe, aplikimet e qelizave diellore dhe diodat që lëshojnë dritë (LED). Komponimet e gjermaniumit përdoren gjithashtu për katalizatorët e polimerizimit dhe së fundmi kanë gjetur përdorim në prodhimin e nanotelave. Ky element formon një numër të madh komponimesh organogermanium, të tilla si tetraethylgermanium, të dobishëm në kiminë organometalike.
Germaniumi nuk mendohet të jetë një element thelbësor për ndonjë organizëm të gjallë. Ngjashëm me silicin dhe aluminin, komponimet natyrale të germaniumit priren të jenë të patretshme në ujë dhe kështu kanë pak toksicitet oral. Megjithatë, kripërat sintetike të tretshme të germaniumit janë nefrotoksike, dhe komponimet sintetike kimikisht reaktive të germaniumit me halogjene dhe hidrogjen janë irritues dhe toksina.]1
Veti e germaniumit (nga Wikipedia)
| Germanium: simboli Ge |
| Pamja: gri-bardhë |
Pesha standarde atomike Ar° (Ge): • 72.630±0.008[1], • 72.630±0.008 (shkurtuar) |
| Germaniumi në tabelën periodike |
| Numri atomik (Z): 32 |
| Grupi: Grupi 14 (Grupi i Karbonit) |
| Periudha: periudha 4 |
| Bllok: Blloku P |
| Konfigurimi i elektroneve: [Ar] 3d10 4s2 4p2 |
| Elektronet për guaskë: 2, 8, 18, 4 |
| Vetitë fizike |
| Faza në STP: e fortë |
| Pika e shkrirjes: 1211.40 K (938.25 °C, 1720.85 °F) |
| Pika e vlimit: 3106 K (2833 °C, 5131 °F) |
| Dendësia (në 20° C): 5.327 g/cm3 , kur është i lëngshëm (në pikë vlimi): 5.60 g/cm3 |
| Nxehtësia e shkrirjes: 36.94 kJ/mol |
| Nxehtësia e avullimit: 334 kJ/mol |
| Kapaciteti i nxehtësisë molare: 23.222 J/(mol· K) |
| Kapaciteti specifik i nxehtësisë: 319.73 J/(kg· K) |
| Presioni i avullit: P (Pa) në T (K) 1 në 1644 10 në 1814 100 në 2023 1 mijë në 2287 10 mijë në 2633 100 mijë në 3104 |
| Vetitë atomike |
| Gjendja e oksidimit, të zakonshme: −4, +2, +4, −3, −2, −1, 0, +1, +3 |
| Elektronegativiteti, Shkalla Pauling: 2.01 |
| Energjitë e jonizimit: • 1: 762 kJ/mol, • 2: 1537.5 kJ/mol, • 3: 3302.1 kJ/mol, • |
| Rrezja atomike, Empirike: 122 pm (pikometer) |
| Rrezja kovalente: 122 pm |
| Rrezja e Van der Waals: 211 pm |
| Veti të tjera |
| Ndodhia natyrore: Primordiale |
| Struktura kristalore: diamant-kub me në qendër fytyrën (cF8) |
| Histori |
| Emërtimi: pas Gjermanisë, atdheu i zbuluesit |
| Parashikimi: Dmitri Mendeleev (1869) |
| Zbulimi: Clemens Winkler (1886) |
| Izotopet e germaniumit: 68Ge, 70Ge, 71Ge, 72Ge, 73Ge, 74Ge, 76Ge |
| f |
Vetit dhe ndodhja
[: Në bazë të peshës, germaniumi është një element i rrallë, por jo jashtëzakonisht i rrallë (rreth 1.5 pjesë për milion) në koren e Tokës, i barabartë me bollëk berilium, molibden dhe cezium dhe tejkalon elementët arsenik, kadmium, antimon dhe merkur. Në kozmos bollëku atomik i germaniumit është 50.5 (bazuar në Si = 1 × 106), një vlerë afërsisht e barabartë me ato për kriptonin dhe zirkonin dhe vetëm pak më pak se ajo për selenin. Bollëku kozmik është shumë më i vogël se ato të një numri elementësh më të rëndë; p.sh., brom, stroncium, kallaj, barium, merkuri dhe plumbi. Të gjithë elementët me ngarkesë bërthamore më të ulët se germaniumi, përveç berilit, borit, skandiumit dhe galiumit, janë kozmikisht më të bollshëm se germaniumi. Kozmikisht, germaniumi besohet të jetë një nga elementët e shumtë të formuar nga thithja e neutroneve pas proceseve fillestare të djegies së hidrogjenit dhe heliumit dhe thithjes së grimcave alfa.
Germaniumi është i shpërndarë gjerësisht në natyrë, por është shumë reaktiv për të ndodhur i lirë. Mineralet kryesore përfshijnë argyrodite (nga i cili u izolua për herë të parë), germanite, renierite dhe canfieldite, të gjitha të rralla; Vetëm germaniti dhe renieriti janë përdorur si burime komerciale për elementin. Sasi të vogla të germaniumit gjenden në disa përzierje zinku, në mineralet sulfidike të bakrit dhe arsenikut dhe në qymyr, kjo e fundit ndoshta një pasojë e përqendrimit të elementit nga bimët e periudhës karbonifere në historinë gjeologjike. Disa bimë të sotme dihet se përqendrojnë germaniumin. Si koncentratet e procesit të zinkut ashtu edhe pluhuri i hirit dhe tymit nga instalimet e djegies së qymyrit sigurojnë burime komerciale të germaniumit.
Në rafinimin e germaniumit, mbetjet e shkallës së ulët të marra nga mineralet e tij trajtohen me acid klorhidrik të fortë, dhe tetrakloruri i germaniumit që rezulton distilohet, pastrohet me ridistilim të përsëritur dhe hidrolizohet për të formuar dioksid germaniumi, i cili më pas reduktohet nga hidrogjeni në një formë pluhur të metalit që shkrihet në një temperaturë prej rreth 1,100° C (2,000° F [në një atmosferë inerte]) dhe hidhet në shufra ose bileta.]2
Historia
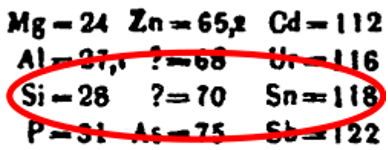
Parashikimi i germaniumit, “?=70” (tabela periodike 1869)
Në raportin e tij mbi Ligjin Periodik të Elementeve Kimike në 1869, kimisti rus Dmitri Mendeleev parashikoi ekzistencën e disa elementëve kimikë të panjohur, duke përfshirë një që do të mbushte një boshllëk në familjen e karbonit, të vendosur midis silikonit dhe kallajit. Për shkak të pozicionit të tij në tabelën e tij periodike, Mendeleev e quajti atë ekasilikon (Es) dhe ai vlerësoi peshën e tij atomike në 70 (më vonë 72).
Referencat